heavy-T2強調/MR angiography 融合画像を用いた脳神経/血管構造において 3TMRIによる3次元画像再構成の有用性 東京大学 医学部 脳神経外科
「我々は3TMRIによる高解像度のSSFPとTOF―MRAの合成2次元データを3次元再構成することで、脳神経と周辺動脈との位置関係を明瞭に描出することに成功した。脳幹周囲構造の立体表示により任意の方向、断面、透過度の設定が可能となり、脳外科手術前シミュレーションとして極めて有用である」
東京大学 医学部 脳神経外科 鎌田恭輔氏、斉藤延人氏
使用製品 Real INTAGE
東京大学 医学部 脳神経外科では、シミュレーション用3D画像作成にReal INTAGEを活用しています。鎌田様、斉藤様にお話をお伺いしました。
脳神経外科手術に臨む際は、術前の画像診断による詳細な検討と、電気生理学的手法による術中機能モニタリングが脳機能温存のために重要である。術前に実際の手術野に近い画像を作成して手術シミュレーションを行うことで、最小限の開頭、くも膜切開を想定しながら、十分な術野を確保することで脳機能損傷を最小限に抑えることができる。
特に後頭蓋窩病変へのアプローチでは、頭蓋底、脳幹、小脳、脳神経、動静脈などが複雑な位置関係を構成しているため、術中のオリエンテーション、操作は細心の注意を払わなければならない。Cadaver による頭蓋底解剖に関する詳細な検討や手術トレーニングコースはすでに確立しているが、患者個々の病変に対する適切なアプローチ、治療方針の決定は、未だに術者の経験に基づいて行われているのが現状である。
脳幹部病変の画像診断は、後頭蓋窩によるアーチファクトの少ないMRI検査が他検査に比して秀でているが、脳神経の描出は困難であった。以前は1.5テスラ装置を用いたgradient echo 法による3次元T1強調画像(3D turbo flip low angle shot〈FLASH〉、3D spoiled gradient echo〈SPGR〉など)が、スライス厚を1.5㎜以下に設定して撮像できるため、用いられていた。しかし、拍動によるgradient echo の揺らぎ、信号・雑音比の低さなどから、視神経、三叉神経以外の脳神経の描出は困難であった。また、この撮像法では繰り返し時間(TR)が短いため、血流に由来するflow void やparadoxicalenhancement(inflow effect)も現れにくく、血管構造の描出には適していなかった。
近年MRI撮像技術の進歩により、完全な定常状態(Steady State Free Precession :SSFP)を保って信号を計測することが可能になった。各社様々な名称(True-FISP, FIESTA,Balanced-FFE, CISS)があるが、本法により保たれる定常状態とは、TRが対象組織のT2よりも十分に短いという条件でRadio frequency(RF)を連続的に印加することで、FID(Free Induction Decay)信号、Spin Echo 信号およびStimulated echo信号が合わさり、横磁化がある一定の状態になることを示す。
取得データは横磁化成分を含んだFID、Spin Echo, Stimulated Echo 信号で構成されているため、結果はT2成分の寄与が大きく、水信号が強調された信号・雑音比のよい画像となる。このような正確なシーケンスタイミングの設定、ハードウェアの確立により、S/Nが高く、組織のT2/T1コントラストに依存する水を強調した画像取得が可能になった。本方法では、水以外の構造物(すべての脳神経、脳神経周囲の血管構造、くも膜など)が低信号となり、また拍動によるアーチファクトも少ないために脳幹周辺の病変の描出に極めて適している。
また、脳幹部周辺の血管情報を取得するためには3次元T1強調画像(3D turbo FLASH、SPGR)法にpreparation pulse を併用することで、time-of-flight 効果を検出する3DTOF MR angiography(TOF―MRA)が適している。
特に後頭蓋窩病変では3Dデータのslab厚を薄く設定できるため、slab 内へのTOF効果が強く保たれていることが期待できる。また、03年2月より国内で3TMRI装置の薬事が承認され、高磁場MRI装置の臨床応用が可能となった。高磁場装置の特徴としては、(1)信号・雑音比がほぼ2倍に向上する、(2)化学シフトの拡大、(3)Susceptibility artifact の増大、(4)組織T1値の延長、(5)Signal abortion ratio(SAR)の増大などがあげられる。3T高磁場MRI装置を用いることで、後頭蓋窩の微小構造をより明瞭に描出が可能になり、前述したSSFP、TOF―MRAなども、より高解像な画像を得ることができる。
また、コンピュータ画像処理技術の発展により、近年はこのように得られた高解像度データを市販のパーソナルコンピュータ上で3次元再構成することも可能になった。SSFP画像を3次元再構成することにより、脳神経と頭蓋底を含む脳幹周囲構造が立体的表示できる。さらにTOF―MRAの情報を加えることで、動脈の解剖学的位置関係が同時に把握することができる。
我々は3TMRIによる高解像度のSSFPとTOF―MRAの合成2次元データを3次元再構成することで、脳神経と周辺動脈との位置関係を明瞭に描出することに成功した。脳幹周囲構造の立体表示により任意の方向、断面、透過度の設定が可能となり、脳外科手術前シミュレーションとして極めて有用であるので、本稿でその詳細を述べる
対象および方法
対象
対象は顔面痙攣、三叉神経痛などの脳神経血管減圧術を受ける患者8例を対象とした。使用機器はGeneral electric 社製Signa 3TMRI 頭部専用装置である。
撮像条件
撮像シーケンスは、GE社のFast Imaging Employing Steady state Acquisition(FIESTA)とTOF―MRA法を用いた。今回の撮像条件をGE社製1.5TMRI装置の条件との比較を、下記の表に示す。
| FIESTA | TOF-MRA | ||
| 1.5T | 3T | 3T | |
| TR(ms) | 8.4 | 5 | 28 |
|---|---|---|---|
| TE(ms) | 2.2 | 1.9 | 3.1 |
| FA | 45 | 45 | 20 |
| No. of Pixels | 256 | 512 | 512 |
| Pixel size(mm) | 0.625 | 0.3906 | 0.3906 |
| FOV(mm) | 160 | 200 | 200 |
| Thickness(mm) | 1 | 0.8 | 0.8 |
| No. of Slices | 60 | 160 | 160 |
| Slab(mm) | 60 | 128 | 128 |
表1
3T装置では1.5T装置に比較してTR/TEがやや短くなっているが、Flip angle(FA)は同じである。また、スライス厚は薄く(0.8㎜)、ピクセルサイズも小さく(0.3906㎜)設定できるため、高解像の画像取得が可能となった。さらに、FIESTAでは脳神経と血管の区別が困難なため、MRAによる血流の情報を加味した。このため、TOF―MRAも同様の解像度で脳幹部を含む領域の座標に一致させて撮像した。
画像合成、および3次元再構成
基本的に撮像時にFIESTAとTOF―MRAの位置座標は同一にしているが、2データの重ね合わせ画像を作成して座標、画像歪みの確認を行った。重ね合わせ画像はDr. View(旭化成)を用いて作成し、座標位置のズレが疑われた際には、FIESTAを基本画像としてMutual information 法によるTOF―MRAの座標位置補正を行った後にDICOMフォーマット画像としてresliceをした。
同一座標のデータセットは、RealIntage(サイバネット)を用いて画像融合(fusion)を行った。まず、TOF―MRAを3次元再構成し、血管情報のみを抽出した。その後FIESTAと抽出したMRAデータのfusion を行い、3次元再構成した。
3次元再構成fusion データでは、FIESTAとTOF―MRAについて独立した信号値を保っているため、それぞれの画像の透過度、強度、色彩を別個に指定することができる(図1)。
Fusion データを任意の方向から3次元再構成し、血管と神経との位置関係を把握することができる。さらに内視鏡モードを用いることで、術中所見に近い視野を得ることが可能となる。
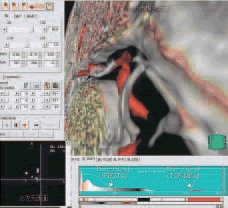
図1 3次元再構成画像ソフトウェアの合成画像とカラーパレット
3次元再構成の結果
画像表示
FIESTAは白、灰色、黒、と黄色を用いたグラデーション、一方、TOF―MRAは赤色として、それぞれ陰影(shading)処理後にカラー表示した(図1)。三叉神経(V)VII(顔面神経)―VIII(蝸牛・前庭神経)complex 近傍部は、任意断面画像により描出した。任意断面処理と画像を回転することにより、神経、血管の位置関係の表示が可能となり、透明度(opacity)は80~100%とした。
解剖学的構造
脳幹前面、V、VII-VIII complex、椎骨―脳底動脈、前下小脳動脈および後下小脳動脈を全例で描出できた。また、Petrosal veinの信号はTOF―MRAでは検出されず、FIESTAでのみ観察できた。
三叉神経痛の症例では、FIESTAでは左SCA周辺に背側から圧迫があることが確認された(図2A)。TOF―MRAでも同様に三叉神経を圧迫するoffending artery の存在が疑われた(図2B)。
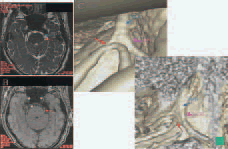
図2 左三叉神経痛症例1
(A)FIESTA:三叉神経背側に圧迫血管を疑わせる所見あり(赤矢印)。
(B)TOFMRA:三叉神経に接している動脈信号あり(赤矢印)。
(C, D)FIESTA の3次元再構成画像:三叉神経に動脈(赤矢印)と
血管様の構造物(ピンク矢印)が圧迫している
FIESTAの3次元再構成画像によると、三叉神経の脳幹近傍部に赤矢印とピンク矢印で示した2ヵ所の圧迫があることが示唆された(図2C、D)。しかし、FIESTAのみでは、再構成角度、拡大率を変えても、その走行からは、動・静脈の鑑別は困難であった。FIESTAとTOF―MRAの2次元fusion 画像(図3A、B)では、三叉神経に接している構造物がTOF―MRAにより動脈と考えられた。3次元再構成したfusion 画像では、三叉神経脳幹部周辺には背側と、腹側の2ヵ所から動脈が圧迫していることが明らかになった(図3C)。
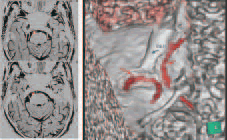
図3 (A, B)FIESTA とTOF-MRA の2次元fusion 画像
(C)Fusion データの3次元再構成画像三叉神経に2ヵ所の動脈の圧迫あり(赤矢印)
図4に術中所見を示す。三叉神経(青矢印)背側にPetrosal vein が存在し、そのやや尾側に下方から圧迫している前下小脳動脈(赤矢印)を認めた。さらに頭腹側側からは上小脳動脈(赤矢印)も圧迫している所見を認めた(図4A)。手術野を想定した視野を設定し、内視鏡モードでfusion 画像を3次元再構成した結果(図4B)では、上述した手術所見と同様にoffending artery が2本存在していた。参考までに実際の手術所見の図を示す(図4C)が、fusion 画像が正確に圧迫部位を表していた。
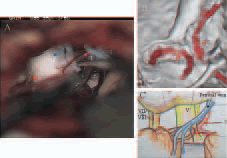
図4
(A)術中所見:三叉神経に2ヵ所の動脈圧迫(赤矢印)あり
(B)Fusion データの3次元再構成画像
(C)手術記載
別の三叉神経痛の症例を示す。術前は三叉神経脳幹側に上小脳動脈が圧迫していた。周辺のvein はFIESTAで灰色に描出されている(図5A)。術中所見でも、動・静脈は三叉神経周辺に複雑に走行していた。しかし、明らかに三叉神経を圧迫していたのは術前画像と同様に上小脳動脈のみが圧迫し、三叉神経に圧痕を認めた(図5B)。減圧術後は三叉神経から上小脳動脈が離れており、上方のテント下面に固定されていることが確認できた(図5C)。本法によりわずかな血管偏位による手術効果を客観的に評価できることができた。
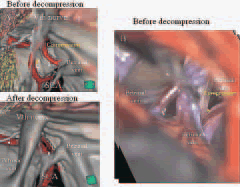
図5 左三叉神経痛症例2
(A)術前fusion データの3次元再構成画像:三叉神経に上小脳動脈の圧迫あり(黄矢印)
(B)術中所見:三叉神経に上内側からSCA の圧迫(赤矢印)あり
(C)術後fusion データの3次元再構成画像:上小脳動脈による三叉神経の圧迫が解除されている
VII-VIII complex はFIESTAのみを用いた3次元再構成画像でも、その走行の特徴より神経と血管との解剖学的関係が把握できる。図6AではVII-VIII complex が明瞭に描出されている。蛇行した椎骨動脈がVIIの脳幹側出口付近を圧迫してることが推察された。
しかし、fusion データの3次元再構成画像(図6B)によると、蛇行した椎骨動脈より後下小脳動脈が分岐し、その分岐部がVII を圧迫していた。術中所見では蛇行した椎骨動脈に圧迫された後下小脳動脈基部がVII を圧迫していた。椎骨動脈のみの偏位による減圧では、操作が不十分となる危険性が予見できた症例であった。
以上のように本方法を用いることにより、脳神経、脳幹周囲の血管を明瞭に描出し、手術シミュレーションとして臨床応用が可能であった。

図6 右顔面痙攣症例
(A)FIESTA の3次元再構成画像:椎骨動脈がVII を圧迫している。
(B)術前fusion データの3次元再構成画像:椎骨動脈と、分枝している後下小脳動脈がVII を圧迫している
現実に近い手術野作成を3次元再構成が可能にする
ハード・ソフトウェアの目覚ましい発展により、FIESTAをはじめとするSSFP系の高速シーケンスの臨床応用が可能になった。すでに、FIESTAにより脳神経を始めとする脳幹周辺構造物を正確に描出できることが報告されている。さらに、3TMRI装置の導入により信号強度の高い画像データを取得することが可能となった。
SSFPはスポイリング技術を用いていないため、TR内に生じるoff-resonancespinの位相のずれが蓄積され続け、位相差による信号の打ち消し合いがブラックバンドアーチファクトを生じさせる。これを回避するためには、磁場の均一性の向上とTRの短縮が必要である。目的部位での十分なshimming の施行と、可能な限り短いTRの設定が必要である。
また、完全な定常状態を達成するには、RF励起ごとの横磁化の相対的な位相分散をゼロにする必要がある。このため、傾斜磁場により生じる位相分散は、極性を反転した傾斜磁場により再びゼロとして、その結果すべての軸の傾斜磁場は、TR間の総和がゼロとなるよう制御が必要である。今後のハード・ソフトウェアの改善、Parallel imaging 法の導入、検出コイルの進歩などにより、より高解像度の画像データの取得が可能になるものと期待される。
本手術シミュレーションでは静脈情報を加えることが未だに困難である。流速の遅い静脈の描出にはPhase contrast 法が、TOF法より感度が高いと考えられるが、脳幹周囲の細い静脈の描出は未だ困難である。むしろ造影剤により信号が増強するTOF―MRAにより静脈信号を検出することが現段階では適切と思われる。しかし、静脈描出のみを目的とした造影剤の使用には慎重に適応を考慮すべきである。また、近年は磁化率の違いを強調したSusceptibility - weighted imaging(SWI)が還元型ヘモグロビンを強調することで静脈を描出することが知られている。
本本法は細い静脈にも高感度で検出することができる。また、磁化率の違いを強調しているため、高磁場装置に適したシーケンスであり、今後さらなる発展が期待できる。以上のように、MRI技術は目覚ましいスピードで進歩しつつある。また、解像度の高いMRIデータを合成し、3次元再構成することで現実に近い手術野を作成することが可能になりつつある。しかし、さらなる手術シミュレーションの発展には、数多くのMRIの撮像原理とその信号の特徴を理解した上で、得られたデータを適切に選択、合成表示していくことが必須である。
お忙しい中、インタビューにご協力いただきまして、誠にありがとうございました。








